承認・届出等
販売名
Tornusトルナス LX
添付文書管理コード
22100BZX01023000_A_01
医療機器承認番号
22100BZX01023000
医療機器承認年月
平成21年10月
一般的名称
一般的名称
46916000
血管狭窄部貫通用カテーテル
禁忌・禁止1.
再使用禁止、再滅菌禁止
1.
時計方向、反時計方向を問わず同方向へ連続して20回転以上回転させないこと。[本品の破損の原因となる。] 2.
ステントストラットを経由する病変には使用しないこと。[本品の破損の原因となる。] 3.
本品を回転操作する場合、両手でコネクタ部を持って連続回転させたり、他の動力源を使用したりしないこと。[本品の破損の原因となる。] 4.
アルコール等、有機溶剤を含む薬剤及び油性造影剤の使用あるいは併用及び浸漬、または拭き取りを行わないこと。[本品の破損の原因となる。]
|
形状・構造及び原理等
形状
1.
本品または併用するガイドワイヤ、カテーテル等の製品ごとの仕様については、各製品ラベルを確認すること。
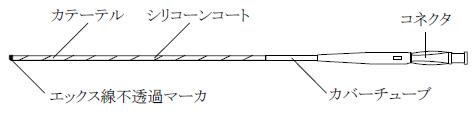
原材料
ステンレス鋼、シリコーン油、プラチナ、ポリアミド樹脂、
ポリカーボネート樹脂
ポリカーボネート樹脂
使用目的又は効果
使用目的
本品は、狭窄性血管(動脈、静脈又はシャント)へのガイドワイヤーの通過が困難な患者に対し、経皮的経血管形成術(PTA)を実施するに際し、ガイドワイヤーの通過部を確保することを目的に使用するカテーテルである。
ただし、狭窄性血管としては、冠血管、頸動脈及び頭蓋内の脳血管を除く。
ただし、狭窄性血管としては、冠血管、頸動脈及び頭蓋内の脳血管を除く。
使用方法等
使用方法
1.
本品をホルダーチューブごと包装から取り出す。
2.
ヘパリン加滅菌生理食塩液を満たしたバットに本品をホルダーチューブごと浸す。
3.
シリンジを用いて、ホルダーチューブのフラッシュコネクタ部からホルダーチューブ内にヘパリン加滅菌生理食塩液を注入する。
(注意)ホルダーチューブ内にヘパリン加滅菌生理食塩液を注入する際は、本品がホルダーチューブから飛び出す可能性があるため、ゆっくりと注入すること
4.
コネクタよりヘパリン加滅菌生理食塩液を注入して気泡を除去する。
5.
ガイドワイヤを本品の内腔に挿入し、慎重に押し進める。
6.
シースイントロデューサ或いは、ガイディングカテーテルに接続されている止血弁を緩め、本品をシースイントロデューサ或いはガイディングカテーテル内に挿入する。
(注意)Yコネクタ等を使用する場合、止血弁による本品シャフト部への過度な締め付けや、締め付けたままでの操作は行わないこと。[本品が破損する可能性がある。]
7.
本品をシースイントロデューサ或いは、ガイディングカテーテルの先端手前までゆっくり進める。
(注意)本品を回転操作する場合は、必ず片手でコネクタ部を持ち、随時溜まった捻りを解放しながら回転させること。溜まった捻りを解放させる際には、必ずYコネクタ等の止血弁を解放させること。
8.
ガイドワイヤのみを目的の血管に挿入し、できるだけ末梢まで進める。
9.
シースイントロデューサ或いはガイディングカテーテルより確認造影を行い、ガイドワイヤが狭窄部を通過していることを確認する。
10.
ガイドワイヤに沿って、本品の先端部を狭窄部に達するまで進める。このとき、本品先端部エックス線不透過マーカを目安とすること。
11.
止血弁を緩めた後、ガイドワイヤ及びシースイントロデューサ或いはガイディングカテーテルを確実に固定し、本品のエックス線不透過マーカを目安に先端が目的部位を通過するまでガイドワイヤに沿って少しずつ押し進める。
12.
必要に応じて8.〜11.の操作を繰り返し、狭窄部を貫通していることを確認する。
13.
手技の終了後、本品を慎重に抜去する。
使用上の注意
重要な基本的注意
1.
本品は、薬液注入には用いないこと。
2.
本品の使用は、緊急の外科手術を行うことができる状況下で行うこと。
3.
本品の操作は、高解像度のエックス線透視下にて製品の動きを確認して行うこと。
4.
術中は患者の状態を考慮して適切な抗凝固療法を行うこと。
5.
親水性コート等(樹脂被覆を含む)が施されたガイドワイヤとは併用しないこと。
6.
本品のすべての操作は、ガイドワイヤ先行下で行うこと。
7.
本品を使用中に異常な抵抗が感じられる場合は、直ちに操作を中止すること。
8.
本品の回転操作時に、コネクタ近位部シャフトを曲げない様に回転操作を加えること。
9.
本品と併用ガイドワイヤとの間に抵抗を感じることがあるため、本品の挿入及び交換時には、本品及び併用ガイドワイヤの表面に付着した血液や造影剤を、ヘパリン加滅菌生理食塩液に浸したガーゼ、脱脂綿等で軽く拭き除去すること。
10.
本品本体部は漏出性があるため、本品内を液体により加圧することができない。そのため、ヘパリン加滅菌生理食塩液の注入圧を利用して本品を抜去する方法(通称:南都法)は用いないこと。
不具合
本品には以下のような不具合が生じる可能性がある。したがって、前述の使用上の注意に記載された事項を守った上で慎重に本品を使用すること。不具合の発生は、有害事象を引き起こす可能性がある。
重大な不具合
・破損(断裂、折れ、曲がり、変形、コーティング剥がれ)
・抜去困難
・挿入困難
有害事象
手技に伴い、以下のような有害事象が生じる可能性がある。有害事象が重篤な場合には重大な合併症を引き起こす可能性がある。
重大な有害事象
・死亡
・感染症
・血管解離
・血管穿孔
・出血性合併症
・遠位部塞栓
・血栓
・梗塞
・残留
・虚血
・不整脈
・血管攣縮
・血圧低下
・アレルギー反応
妊婦、産婦、授乳婦及び小児等への適用
1.
本品はエックス線透視下で使用するため、妊娠または妊娠している可能性のある患者に対しては、治療上の有益性が危険性を上回ると判断される場合にのみ使用すること。
保管方法及び有効期間等
保管方法
保管の際には、曲げたり重い物の下に置いたりせず、また水ぬれに注意し、高温、高湿、直射日光を避けること。
有効期間
本品の製品ラベルに記載されている「有効期限」までに使用すること。[自己認証(当社データによる)]
製造販売業者及び製造業者の氏名又は名称等
朝日インテック株式会社
第一種医療機器製造販売業
住所
愛知県瀬戸市暁町3番地100
電話番号
0561-48-5551
その他の安全性情報
備考
規格書番号
AMK-DT152 Ver.2.10
AMK-DT152 Ver.2.10