トリキュラー錠21/トリキュラー錠28
作成又は改訂年月
| * | 2020年 6月改訂 ( 第1版 ) |
日本標準商品分類番号
薬効分類名
承認等
トリキュラー錠21
販売名コード
YJコード
販売名英語表記
販売名ひらがな
承認番号等
承認番号
販売開始年月
貯法・有効期間
貯法
有効期間
規制区分
処方箋医薬品 注)
注) 注意―医師の処方箋により使用することトリキュラー錠28
販売名コード
YJコード
販売名英語表記
販売名ひらがな
承認番号等
承認番号
販売開始年月
貯法・有効期間
貯法
有効期間
規制区分
処方箋医薬品 注)
注) 注意―医師の処方箋により使用すること一般的名称
なお、必要に応じ、性感染症検査の実施を考慮すること。
2. 禁忌(次の患者には投与しないこと)
- 2.1 本剤の成分に対し過敏性素因のある女性
- 2.2 エストロゲン依存性悪性腫瘍(例えば、乳癌、子宮内膜癌)、子宮頸癌及びその疑いのある患者[腫瘍の悪化あるいは顕性化を促すことがある。],,
- 2.3 診断の確定していない異常性器出血のある患者[性器癌の疑いがある。出血が性器癌による場合は、癌の悪化あるいは顕性化を促すことがある。],
- 2.4 血栓性静脈炎、肺塞栓症、脳血管障害、冠動脈疾患又はその既往歴のある患者[血液凝固能が亢進され、これらの症状が増悪することがある。]
- 2.5 35歳以上で1日15本以上の喫煙者[心筋梗塞等の心血管系の障害が発生しやすくなるとの報告がある。],,,
- 2.6 前兆(閃輝暗点、星型閃光等)を伴う片頭痛の患者[前兆を伴う片頭痛の患者は前兆を伴わない患者に比べ脳血管障害(脳卒中等)が発生しやすくなるとの報告がある。]
- 2.7 肺高血圧症又は心房細動を合併する心臓弁膜症の患者、亜急性細菌性心内膜炎の既往歴のある心臓弁膜症の患者[血栓症等の心血管系の障害が発生しやすくなるとの報告がある。],
- 2.8 血管病変を伴う糖尿病患者(糖尿病性腎症、糖尿病性網膜症等)[血栓症等の心血管系の障害が発生しやすくなるとの報告がある。]
- 2.9 血栓性素因のある女性[血栓症等の心血管系の障害が発生しやすくなるとの報告がある。]
- 2.10 抗リン脂質抗体症候群の患者[血栓症等の心血管系の障害が発生しやすくなるとの報告がある。]
- 2.11 手術前4週以内、術後2週以内、産後4週以内及び長期間安静状態の患者[血液凝固能が亢進され、心血管系の副作用の危険性が高くなることがある。],
- 2.12 重篤な肝障害のある患者
- 2.13 肝腫瘍のある患者[症状が増悪することがある。]
- 2.14 脂質代謝異常のある患者[血栓症等の心血管系の障害が発生しやすくなるとの報告がある。また、脂質代謝に影響を及ぼす可能性があるため、症状が増悪することがある。]
- 2.15 高血圧のある患者(軽度の高血圧の患者を除く)[血栓症等の心血管系の障害が発生しやすくなるとの報告がある。また、症状が増悪することがある。],
- 2.16 耳硬化症の患者[症状が増悪することがある。]
- 2.17 妊娠中に黄疸、持続性そう痒症又は妊娠ヘルペスの既往歴のある患者[症状が再発するおそれがある。]
- 2.18 妊婦又は妊娠している可能性のある女性,,
- 2.19 授乳婦
- 2.20 骨成長が終了していない可能性がある女性[骨端の早期閉鎖を来すおそれがある。]
3. 組成・性状
3.1 組成
トリキュラー錠21
| 有効成分 | レボノルゲストレル(1錠中) 0.050mg |
|---|---|
| 日局エチニルエストラジオール(1錠中) 0.030mg | |
| 添加剤 | ステアリン酸マグネシウム、ポビドン、タルク、マクロゴール6000、モンタン酸エステルワックス、沈降炭酸カルシウム、精製白糖、乳糖水和物、トウモロコシデンプン、グリセリン、酸化チタン、黄色三二酸化鉄、三二酸化鉄 |
| 錠数 | 6錠 |
| 有効成分 | レボノルゲストレル(1錠中) 0.075mg |
|---|---|
| 日局エチニルエストラジオール(1錠中) 0.040mg | |
| 添加剤 | ステアリン酸マグネシウム、ポビドン、タルク、マクロゴール6000、モンタン酸エステルワックス、沈降炭酸カルシウム、精製白糖、乳糖水和物、トウモロコシデンプン |
| 錠数 | 5錠 |
| 有効成分 | レボノルゲストレル(1錠中) 0.125mg |
|---|---|
| 日局エチニルエストラジオール(1錠中) 0.030mg | |
| 添加剤 | ステアリン酸マグネシウム、ポビドン、タルク、マクロゴール6000、モンタン酸エステルワックス、沈降炭酸カルシウム、精製白糖、乳糖水和物、トウモロコシデンプン、グリセリン、酸化チタン、黄色三二酸化鉄 |
| 錠数 | 10錠 |
トリキュラー錠28
| 有効成分 | レボノルゲストレル(1錠中) 0.050mg |
|---|---|
| 日局エチニルエストラジオール(1錠中) 0.030mg | |
| 添加剤 | ステアリン酸マグネシウム、ポビドン、タルク、マクロゴール6000、モンタン酸エステルワックス、沈降炭酸カルシウム、精製白糖、乳糖水和物、トウモロコシデンプン、グリセリン、酸化チタン、黄色三二酸化鉄、三二酸化鉄 |
| 錠数 | 6錠 |
| 有効成分 | レボノルゲストレル(1錠中) 0.075mg |
|---|---|
| 日局エチニルエストラジオール(1錠中) 0.040mg | |
| 添加剤 | ステアリン酸マグネシウム、ポビドン、タルク、マクロゴール6000、モンタン酸エステルワックス、沈降炭酸カルシウム、精製白糖、乳糖水和物、トウモロコシデンプン |
| 錠数 | 5錠 |
| 有効成分 | レボノルゲストレル(1錠中) 0.125mg |
|---|---|
| 日局エチニルエストラジオール(1錠中) 0.030mg | |
| 添加剤 | ステアリン酸マグネシウム、ポビドン、タルク、マクロゴール6000、モンタン酸エステルワックス、沈降炭酸カルシウム、精製白糖、乳糖水和物、トウモロコシデンプン、グリセリン、酸化チタン、黄色三二酸化鉄 |
| 錠数 | 10錠 |
| 有効成分 | レボノルゲストレル(1錠中) 含有せず |
|---|---|
| 日局エチニルエストラジオール(1錠中) 含有せず | |
| 添加剤 | ステアリン酸マグネシウム、ポビドン、タルク、マクロゴール6000、モンタン酸エステルワックス、沈降炭酸カルシウム、精製白糖、乳糖水和物、トウモロコシデンプン |
| 錠数 | 7錠 |
4. 効能又は効果
避妊
6. 用法及び用量
7. 用法及び用量に関連する注意
- 7.1 毎日一定の時刻に服用させること。
-
7.2 服用開始日
経口避妊剤を初めて服用させる場合、月経第1日目から服用を開始させる。服用開始日が月経第1日目から遅れた場合、飲みはじめの最初の1週間は他の避妊法を併用させること。 -
7.3 本剤の投与にあたっては飲み忘れ等がないよう服用方法を十分指導すること。万一飲み忘れがあった場合(28錠製剤の白色糖衣錠(大)を除く)、翌日までに気付いたならば直ちに飲み忘れた錠剤を服用し、その日の錠剤も通常どおりに服用させる。
2日以上連続して飲み忘れがあった場合は服用を中止させ、次の月経を待ち投与を再開させること。なお、飲み忘れにより妊娠する可能性が高くなるので、その周期は他の避妊法を使用させること。 - 7.4 他の経口避妊剤から本剤に切り替える場合
8. 重要な基本的注意
- 8.1 本剤の服用により、年齢、喫煙、肥満、家族歴等のリスク因子の有無にかかわらず血栓症があらわれることがあるので、次のような症状があらわれた場合は直ちに投与を中止し、適切な処置を行うこと。
- 8.2 本剤の服用中に、血栓症が疑われる症状があらわれた場合は、投与を中止するなど適切な処置を行うこと。
- 8.3 血栓症のリスクが高まる状態(体を動かせない状態、顕著な血圧上昇、脱水等)が認められる場合は、投与を中止するなど適切な処置を行うこと。
- 8.4 本剤服用者には、投与開始時及び継続時に以下について説明すること。
- 8.5 本剤服用中にやむを得ず手術が必要と判断される場合には、血栓症の予防に十分配慮すること。,
- 8.6 年齢及び喫煙量により心血管系の重篤な副作用の危険性が増大するとの報告がある。従って、本剤服用者には禁煙するよう指導すること。,,,
- 8.7 本剤の投与にあたっては服用者の病歴調査及び検診が必要である。この検診には、血圧測定、乳房・腹部の検査及び臨床検査が含まれる。また、投与中は6ヵ月ごとの検診を行うこと。
- 8.8 本剤投与開始前及び投与中は、1年に1回以上、子宮・卵巣を中心とした骨盤内臓器の検査を行うこと。1年に1回、子宮頸部の細胞診の実施を考慮すること。,,
- 8.9 乳癌の検査は、服用者に自己検診を行うよう指導すること。,,
- 8.10 服用中に不正性器出血が発現した場合、通常は投与継続中に消失するが、長期間持続する場合は、腟細胞診等の検査で悪性疾患によるものではないことを確認の上、投与すること。,
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
- 9.1.1 40歳以上の女性(ただし、1日15本以上の喫煙者には投与しないこと)
- 9.1.2 子宮筋腫のある患者
- 9.1.3 乳癌の既往歴のある女性
-
9.1.4 乳癌の家族歴又は乳房に結節のある女性
定期的に乳房検診を行うなど慎重に投与すること。エストロゲン投与と乳癌発生との因果関係についてその関連性を示唆する報告もある。
- 9.1.5 喫煙者(ただし、35歳以上で1日15本以上の喫煙者には投与しないこと)
- 9.1.6 肥満の女性
- 9.1.7 血栓症の家族歴を持つ女性
- 9.1.8 前兆を伴わない片頭痛の患者
- 9.1.9 心臓弁膜症の患者(ただし、肺高血圧症又は心房細動を合併する心臓弁膜症の患者、亜急性細菌性心内膜炎の既往歴のある心臓弁膜症の患者には投与しないこと)
- 9.1.10 軽度の高血圧(妊娠中の高血圧の既往も含む)のある患者
-
9.1.11 耐糖能の低下している女性(糖尿病患者及び耐糖能異常の女性)
十分コントロールを行いながら投与すること。耐糖能が低下することがある。
-
9.1.12 ポルフィリン症の患者
症状が増悪することがある。
-
9.1.13 心疾患又はその既往歴のある患者
ナトリウム又は体液の貯留により症状が増悪することがある。
-
9.1.14 てんかん患者
症状が増悪することがある。
-
9.1.15 テタニーのある患者
症状が増悪することがある。
9.3 肝機能障害患者
9.4 生殖能を有する者
9.5 妊婦
10. 相互作用
10.2 併用注意(併用に注意すること)
| 薬剤名等 | 臨床症状・措置方法 | 機序・危険因子 |
|---|---|---|
|
これらの薬剤の作用が増強するおそれがある。 |
本剤はこれらの薬剤の代謝を抑制すると考えられる。 |
|
|
テオフィリン チザニジン塩酸塩 |
これらの薬剤の血中濃度が上昇するおそれがある。 |
本剤がこれらの薬剤の代謝酵素(CYP1A2)を阻害すると考えられる。 |
|
本剤の効果の減弱化及び不正性器出血の発現率が増大するおそれがある。 |
これらの薬剤は薬物代謝酵素を誘導し、本剤の代謝を促進すると考えられる。 |
|
|
本剤の効果の減弱化及び不正性器出血の発現率が増大するおそれがある。 |
これらの薬剤は腸内細菌叢を変化させ、本剤の腸肝循環による再吸収を抑制すると考えられる。 |
|
|
テルビナフィン塩酸塩 |
黄体ホルモン・卵胞ホルモン配合剤との併用で、月経異常があらわれたとの報告がある。 |
機序不明 |
|
これらの薬剤の作用を減弱するおそれがある。 |
これらの薬剤は性ホルモンの分泌を低下することにより薬効を示すため、性ホルモンである本剤の投与によってこれらの薬剤の効果を減弱する可能性が考えられる。 |
|
|
血糖降下剤の作用が減弱するおそれがある。血糖値その他患者の状態を十分観察し、血糖降下剤の用量を調節するなど注意する。 |
本剤は耐糖能を低下させ、血糖降下剤の作用を減弱させると考えられる。 |
|
|
ラモトリギン モルヒネ サリチル酸 |
これらの薬剤の血中濃度が低下するおそれがある。 |
本剤はこれらの薬剤のグルクロン酸抱合を促進すると考えられる。 |
|
本剤の作用が減弱するおそれがある。 |
エチニルエストラジオールのAUCが減少する。 |
|
|
本剤の血中濃度が上昇するおそれがある。 |
*本剤の代謝酵素(CYP3A4)を阻害すると考えられる。 |
|
|
本剤の血中濃度が上昇するおそれがある。 |
エトラビリンは本剤の代謝酵素(CYP2C9)を阻害すると考えられる。 |
|
|
フルコナゾール |
本剤の血中濃度が上昇するおそれがある。 |
フルコナゾールは本剤の代謝酵素(CYP3A4)を阻害すると考えられる。 |
|
ボリコナゾール |
本剤の血中濃度が上昇するおそれがある。 |
ボリコナゾールは本剤の代謝酵素(CYP3A4)を阻害すると考えられる。 |
|
アセトアミノフェン |
本剤の血中濃度が上昇するおそれがある。 |
アセトアミノフェンはエチニルエストラジオールの硫酸抱合を阻害すると考えられる。 |
|
セイヨウオトギリソウ(St. John's Wort、セント・ジョーンズ・ワート)含有食品 |
本剤の効果の減弱化及び不正性器出血の発現率が増大するおそれがあるので、本剤投与時はセイヨウオトギリソウ含有食品を摂取しないよう注意すること。 |
この食品は薬物代謝酵素を誘導し、本剤の代謝を促進すると考えられる。 |
11. 副作用
11.1 重大な副作用
11.2 その他の副作用
|
5%以上 |
1~5%未満 |
1%未満 |
頻度不明 |
|
|---|---|---|---|---|
|
過敏症 |
発疹、じん麻疹 | |||
|
眼 |
網膜血流障害による視力障害 |
|||
|
肝臓 |
肝機能異常 |
黄疸 |
||
|
電解質代謝 |
浮腫、体重増加 | |||
|
子宮 |
下腹部痛 |
帯下の増加、カンジダ膣炎 |
不正性器出血(破綻出血、点状出血) |
|
|
乳房 |
乳房緊満感 |
乳房痛 | ||
|
循環器 |
動悸、血圧上昇 | |||
|
消化器 |
悪心(29.4%)、嘔吐 |
下痢、腹痛 |
便秘、食欲不振、食欲亢進、口内炎、口渇 | |
|
精神神経系 |
頭痛 |
めまい、片頭痛、神経過敏 |
眠気、抑うつ | |
|
皮膚 |
ざ瘡 |
褐色斑、湿疹 |
色素沈着 注1) |
|
|
その他 |
腰痛、倦怠感・疲労 |
肩こり、息切れ、性欲減退、鼻出血 |
しびれ、総コレステロール上昇、トリグリセリド上昇 |
12. 臨床検査結果に及ぼす影響
含有するエチニルエストラジオールの作用による血清タンパク(コルチコイド結合性グロブリン、サイロキシン結合性グロブリン等)の増加により、総コルチゾール、総T3、総T4の上昇がみられることがある。また、これらの遊離型は変化しないとされている。これら検査値の判定に際しては注意すること。
14. 適用上の注意
15. その他の注意
15.1 臨床使用に基づく情報
- 15.1.1 外国の疫学調査の結果、静脈血栓症のリスクは、経口避妊剤を服用している女性は服用していない女性に比し、3.25~4.0倍高くなるとの報告がある。また、静脈血栓症のリスクは経口避妊剤服用開始の最初の1年間において最も高くなるとの報告がある。さらに、外国での大規模市販後調査の結果、初めて経口避妊剤の服用を開始した時だけでなく、4週間以上の中断後に服用を再開した時又は4週間以上の中断後に別の経口避妊剤へ切り替えた時にも静脈血栓症のリスクが上昇し、そのリスクは服用開始後3ヵ月間が特に高いとの報告がある。
- 15.1.2 外国での疫学調査の結果、経口避妊剤の服用により乳癌及び子宮頸癌になる可能性が高くなるとの報告がある。
- 15.1.3 外国で、経口避妊剤を2年以上服用した場合、良性肝腫瘍が10万人当たり3.4人発生するとの報告がある。また、腫瘍の破裂により腹腔内出血を起こす可能性がある。一方、悪性肝腫瘍(肝癌)の発生率は極めて低く、100万人当たり1人に満たない。
- 15.1.4 外国で、経口避妊剤の服用により全身性エリテマトーデス(SLE)の悪化、アナフィラキシー、溶血性尿毒症症候群(HUS)があらわれたとの報告がある。
- 15.1.5 外国で、経口避妊剤の服用による角膜厚の変化等によりコンタクトレンズがうまく調整されないため、視力・視野の変化、装用時の不快感等がみられたとの報告がある。
16. 薬物動態
16.1 血中濃度
健康女性(8名)に月経第1日より21日間連続経口投与したとき、21日目におけるレボノルゲストレルの血中濃度は、投与1.3時間後に最高値6.18ng/mLを示したのち、22.1時間の半減期で低下した。なお、エチニルエストラジオールは、投与1.6時間後に最高血中濃度121.5pg/mLを示し、半減期は11.2時間であった。
連続投与によるレボノルゲストレル及びエチニルエストラジオールの蓄積はほとんどないものと考えられる1)
。
17. 臨床成績
17.1 有効性及び安全性に関する試験
-
17.1.1 国内臨床試験
避妊を希望する女性を対象とした国内一般臨床試験及び長期投与試験で、投与1周期以上の総計924例(13862周期)で避妊効果が評価された。飲み忘れがあったのは362例(943周期)であり、このうち3錠以上を飲み忘れた4例で妊娠が認められた。薬剤効果不十分による妊娠例は認められなかった2) ,3) ,4) 。
955例中486例(50.9%)に副作用が認められ、主な副作用は、悪心281件(29.4%)、乳房緊満感181件(19.0%)、頭痛143件(15.0%)、嘔吐100件(10.5%)、下腹部痛62件(6.5%)等であった。周期数では13943周期中、1746周期(12.5%)に副作用が認められた。周期数別副作用の発現頻度は、1周期では38.7%、6周期では12.7%、12周期では8.7%で周期が進むにつれて減少した。
17.3 その他
各種避妊法使用開始1年間の失敗率(妊娠率)は以下のとおりである5) 。
|
方法 |
理想的な使用※1
|
一般的な使用※2
|
|
経口避妊剤 |
0.3 |
9 |
|
レボノルゲストレル放出IUS |
0.2 |
0.2 |
|
銅付加IUD |
0.6 |
0.8 |
|
コンドーム |
2 |
18 |
|
リズム法 |
0.4~5 |
24 |
|
女性避妊手術 |
0.5 |
0.5 |
|
男性避妊手術 |
0.10 |
0.15 |
|
避妊せず |
85 |
85 |
|
IUS:子宮内システム IUD:子宮内避妊用具 ※1:選んだ避妊法を正しく続けて使用しているにもかかわらず妊娠してしまった場合 ※2:選んだ避妊法を使用しているにもかかわらず妊娠してしまった場合(経口避妊剤については、飲み忘れを含めた場合の失敗率) |
||
|---|---|---|
18. 薬効薬理
18.1 作用機序
本剤は排卵抑制作用を主作用とし、子宮内膜変化による着床阻害作用及び頸管粘液変化による精子通過阻害作用等により避妊効果を発揮する。
18.2 排卵抑制作用
健康女性(8例)で本剤投与前周期及び投与周期の血清ホルモン動態を検討した。いずれの症例においても、黄体形成ホルモン(LH)及び卵胞刺激ホルモン(FSH)のピークは投与周期に消失した。また、エストラジオールの典型的な2峰性パターン、排卵後のプロゲステロンの上昇も投与周期において抑制され、排卵は抑制されていた1) 。
18.3 子宮内膜の性状変化による着床阻害作用
健康女性(28例)で本剤投与中に子宮内膜診を行った。その組織像は周期的な変化が認められたが、正常周期のものとは異なっていた6) 。
18.4 子宮頸管粘液の変化による精子通過阻害作用
健康女性(6例)で本剤投与中の子宮頸管粘液を調べた。投与中の電子顕微鏡像は黄体期と類似の構造を示し、分泌量も少なく非常に粘性が高かった。また、精子通過性は抑制されていた7) 。
19. 有効成分に関する理化学的知見
レボノルゲストレル
一般的名称
レボノルゲストレル(Levonorgestrel)
化学名
(-)-13-Ethyl-17-hydroxy-18,19-dinor-17α-pregn-4-en-20-yn-3-one
分子式
C21H28O2
分子量
312.45
性状
本品は白色の結晶性の粉末である。
本品はテトラヒドロフラン又はクロロホルムにやや溶けやすく、アセトニトリル、メタノール、エタノール(99.5)、アセトン又はジエチルエーテルに溶けにくく、水にほとんど溶けない。
化学構造式
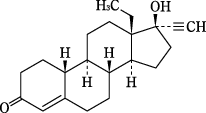
融点
235~241℃
エチニルエストラジオール
一般的名称
エチニルエストラジオール(Ethinylestradiol)
化学名
17α-Ethynylestra-1,3,5(10)-triene-3,17β-diol
分子式
C20H24O2
分子量
296.40
性状
本品は白色~微黄色の結晶又は結晶性の粉末で、においはない。
本品はピリジン又はテトラヒドロフランに溶けやすく、エタノール(95)又はジエチルエーテルにやや溶けやすく、水にほとんど溶けない。本品は水酸化ナトリウム試液に溶ける。
化学構造式
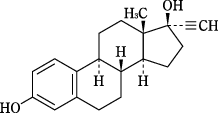
融点
180~186℃又は142~146℃
20. 取扱い上の注意
小児の手のとどかない所に保管するよう指導すること。
22. 包装
23. 主要文献
1) 本庄英雄他: 基礎と臨床. 1991; 25: 999-1021
2) 松本清一他: 基礎と臨床. 1991; 25: 1155-1177
3) 八神喜昭他: 基礎と臨床. 1991; 25: 1178-1191
4) 黄宏駿他: Prog Med. 1991; 11: 349-361
6) Brosens IA: Benefits and Risks of Hormonal Contraception. Lancaster. MTP Press. 1982; 135-142
7) Ulstein M, et al.: Acta Obstet Gynecol Scand. 1982; Suppl 105: 45-49
24. 文献請求先及び問い合わせ先
文献請求先
バイエル薬品株式会社・メディカルインフォメーション
〒530-0001大阪市北区梅田二丁目4番9号
バイエル医療用医薬品のお問い合わせ先
電話0120-106-398
25. 保険給付上の注意
本剤は保険給付の対象とならない(薬価基準未収載)。
26. 製造販売業者等
26.1 製造販売元
バイエル薬品株式会社
大阪市北区梅田二丁目4番9号