薬効分類名
体外診断用医薬品
一般的注意事項
ご使用に際しては、本添付文書をよくお読みください。
承認・届出等
販売名
IOテストFITC標識抗体 HLA-DR IOT2a
添付文書管理コード
20200EZY00112000_Q_01
製造販売承認番号
20200EZY00112000
承認・認証年月等
平成2年8月
一般的名称
一般的名称
80009002
クラスII免疫検査用シリーズ
警告(記載なし)
|
重要な基本的注意(記載なし)
|
全般的な注意
1.
本品は、体外診断用でありそれ以外の目的に使用しないでください。
2.
診断は他の関連する検査結果や臨床症状等に基づいて総合的に判断してください。
3.
添付文書等に記載した内容以外の方法で使用した場合には、保証しません。
4.
ご使用にあたっては、測定装置の取扱説明書をよく読んでから使用してください。
形状・構造等(キットの構成)
構成試薬名
成分
【対象抗原】
【クローン(アイソタイプ及び免疫原)】
【標識】
IOテストFITC標識抗体 HLA-DR IOT2a
成分
FITC標識マウスモノクローナル抗体IgG画分
IOテストFITC標識抗体の各製品は、FITC(isothyocyanate)で標識したマウスモノクローナル抗体試薬(溶液)で、1テストあたり100μLの全血を染色するのに十分な量の抗体タンパクを含有しています。
【対象抗原】
HLA-DR(分子量29/34kD)
B8.12.2抗体は、MHCクラスII抗原の非多型性部位を認識しています。HLA-DR抗原は、T細胞とB細胞、T細胞とマクロファージ間の細胞間協調などに関与しています。HLA-DR抗原は、末梢血のB細胞に強く、単球に弱く発現しています。顆粒球、血小板には発現していません。休止期のT細胞には発現せず、活性化に伴い発現が認められます。
B8.12.2抗体は、MHCクラスII抗原の非多型性部位を認識しています。HLA-DR抗原は、T細胞とB細胞、T細胞とマクロファージ間の細胞間協調などに関与しています。HLA-DR抗原は、末梢血のB細胞に強く、単球に弱く発現しています。顆粒球、血小板には発現していません。休止期のT細胞には発現せず、活性化に伴い発現が認められます。
【クローン(アイソタイプ及び免疫原)】
HLA-DR : B8.12.2(マウスIgG2b、HLA-A6拘束性CTLクローンで免疫)
【標識】
FITC : Fluorescein isothyocyanate
励起波長 485〜509nm、 蛍光波長 504〜541nm
励起波長 485〜509nm、 蛍光波長 504〜541nm
使用目的
HLA-DR : 白血球細胞表面抗原【HLA-DR】(HLA-DR 抗原陽性細胞)の測定
測定原理
測定方法は、フローサイトメトリーを用いた直接免疫蛍光法です。細胞にFITC(緑色蛍光色素)で標識した抗体を反応させ、フローサイトメーターを用いて各抗体の陽性細胞の計測を行います。
操作上の注意
1.
IOテストは、フローサイトメトリー用の抗体試薬です。
2.
抗凝固剤としてEDTA、ヘパリン等を用いることができますが、いずれの場合も採血後は室温で保存します。
3.
長時間(おおむね採血後6時間以上)検体を保存する場合は、検体の安定性についてあらかじめ検討してください。
4.
溶血不良となるおそれがあるため、血液を試験管に分注する際は試験管の上部壁面に血液を付けないよう注意してください。付着した血液は、綿棒等で取り除いてください。
5.
有核赤血球、蛋白濃度が異常な場合、ヘモグロビン合成異常等では、赤血球の溶血が不完全となる場合があります。この場合、溶血していない赤血球を白血球としてカウントするために陽性率が実際よりも低くなるおそれがあります。
6.
溶血時間が長すぎると白血球にも影響が及ぶことがあります。
7.
Ficoll-Paque分離液による単核細胞の比重遠心分離に伴い、白血球中の特定の細胞集団が選択的に失われることがあります。
8.
フローサイトメーターの調整不良、感度やゲート等の不適切な設定により、誤った結果が得られる場合があります。
9.
サンプル調製方法や試薬、フローサイトメーターの機種や測定条件などの違いにより測定値が影響を受けるおそれがあるため、正常参考値は施設ごとに設定してください。
10.
各々の白血球細胞集団の変動は必ずしも病態と一致するとは限らないため、測定結果は臨床所見及び他の検査データと共に使用してください。
11.
測定結果の解釈を行う場合には、測定条件及び供血者の年令、性別、喫煙習慣等の影響も考慮してください。
用法・用量(操作方法)
1.
試薬の調製
モノクローナル抗体試薬はそのまま使用できます(20μL/テスト)。
【その他必要な試薬】
1)
PBS(リン酸緩衛生理食塩水)PBSバッファ(製品番号 6603369)1パックを蒸留水500mLに溶解します。調製後のpHは7.2±0.2で、防腐剤等は含んでいません。ウシ血清アルブミン(BSA、終濃度0.5%)やアジ化ナトリウム(終濃度0.1%)等を添加したものも使用可能です。
2)
ホルムアルデヒド加PBS溶血試薬(下記)にVersaLyseを用いる場合は、PBS 1mLに対しIOTest 3固定試薬(製品番号 A07800)12.5μLの割合で希釈します(0.1%ホルムアルデヒド加PBS)。
VersaLyse以外の溶血試薬を用いる場合は、PBS 1mLに対し IOTest 3固定試薬(製品番号 A07800)67.5μLの割合で希釈します(0.5%ホルムアルデヒド加PBS)。
VersaLyse以外の溶血試薬を用いる場合は、PBS 1mLに対し IOTest 3固定試薬(製品番号 A07800)67.5μLの割合で希釈します(0.5%ホルムアルデヒド加PBS)。
3)
溶血試薬以下のフローサイトメトリー用溶血試薬のいずれかを使用してください。溶血試薬は添付の取扱説明書に従って調製、使用してください。
製品番号 A09777 VersaLyse溶血試薬
製品番号 IM1400 OptiLyse B(他社フローサイトメーター用)
製品番号 A11895 OptiLyse C(ベックマン・コールター社フローサイトメーター用)
製品番号 A07799 IOTest 3溶血試薬
製品番号 IM1400 OptiLyse B(他社フローサイトメーター用)
製品番号 A11895 OptiLyse C(ベックマン・コールター社フローサイトメーター用)
製品番号 A07799 IOTest 3溶血試薬
4)
コントロール試薬(アイソタイプコントロール抗体)
IOTest IgG2b-FITC
製品番号IM1267 容量100テスト(2mL)
5)
Ficoll-Paque分離液Phamacia カタログ番号17-0840-03または相当品を使用してください。
2.
全血サンプルを検体とする場合(全血法)
【検体の採取と調整】
【染色操作法】
試験管1本につき100μLの血液を必要とします。
抗体の染色に最適な白血球数が5×103個/mm3であるため、
白血球数が10×103個/mm3を超える場合は、PBSで検体を希釈し、3×103/mm3より少ない場合には、以下の手順で白血球を濃縮します。
白血球濃縮方法(バフィーコート回収法)
a.
検体を25℃で500×g、5分間遠心分離します。
b.
白血球の層をパスツールピペットで採取します。その際に、すべての白血球を確実に回収するため赤血球及び血漿も一部回収します。
c.
数回ピペッティングして、十分に懸濁させます。
d.
ユニセルDxH800等のヘマトロジーアナライザーや血球計算板を用いて白血球数を測定します。
e.
PBSで白血球数を5〜10×103個/mm3の範囲に調整します。
【染色操作法】
1)
抗体反応用と対照用に12mmφ×75mmの試験管を用意します。
2)
各々の試験管に全血100μLを分注します。管壁に付着した血液は綿棒等で拭き取ってください。
3)
モノクローナル抗体試薬20μLを反応用の試験管に添加します。対照用の試験管には、コントロール試薬(IOTest IgG1-FITCなど、別売)を20μL加えます。
4)
よく攪拌し、室温、暗所で15分間反応させます。
5)
赤血球を溶血させます。用いる溶血試薬の取扱説明書に従って、溶血処理を行ってください。
6)
溶血が完了(サンプルの濁りが消える)したら、PBSを2mL加え、攪拌します。
7)
400×g、3分間遠心分離した後、上清を吸引除去します。
8)
6)〜7)の操作を繰り返します。
9)
沈渣に適量(0.5〜1mL)の0.1%(または0.5%)ホルムアルデヒド加PBSを加え、よく攪拌します。
10)
フローサイトメーターで目的の細胞の蛍光陽性率を測定します。
サンプルはアイスバス中で遮光保存し、24時間以内に測定してください。
3.
Ficoll-Paque 分離単核細胞を検体とする場合
【検体の採取と調整】
【染色操作法】
1)
試験管に血液(抗凝固剤を含む)を3〜4mLとり、ほぼ等量のPBSを加え転倒混和します。
2)
別の試験管にFicoll-Paque分離液を4mL入れ、その上に1)の希釈血液を重層します。
3)
2〜8℃で400×g(分離液により異なる)、30分間遠心分離します。
4)
Ficoll-Paque分離液と血漿の間の層(単核球層)をパスツールピペットで採取し、別の試験管に移します。
5)
PBSを加えて攪拌し、2〜8℃で400×g、8分間遠心分離します。
6)
上清を吸引除去し、沈渣にPBSを加えてよく攪拌します。
7)
2〜8℃で400×g、4分間遠心分離します。
8)
上清を吸引除去し、沈渣にPBSを加えてよく攪拌します。
9)
2〜8℃で400×g、3分間遠心分離します。
10)
上清を吸引除去し、沈渣にPBSを加えて細胞濃度を5×103個/mm3(5×106個/mL)に調整します。
11)
トリパンブルー等で、細胞のバイアビリティ(生残率)をチェックします。バイアビリティは90%以上が適当ですが、検体によってはこれを下回ることがあります。
【染色操作法】
1)
抗体反応用と対照用に12mmφ×75mmの試験管を用意します。
2)
各々の試験管にFicoll-Paque調製サンプルを5×105個(細胞濃度が5×106個/mLの場合 100μL)ずつ分注します。
3)
モノクローナル抗体試薬20μLを反応用の試験管に添加します。対照用の試験管には、コントロール試薬(IOTest IgG1-FITCなど、別売)を20μL加えます。
4)
よく攪拌し、2〜8℃、暗所で30分間反応させます。
5)
PBS 2mLを加え、2〜8℃で400×g、5分間遠心分離し、上清を吸引除去します。
6)
ステップ5)の操作を繰り返します。
7)
適量(0.5〜1mL)の0.5%ホルムアルデヒド加PBSを加え、よく攪拌します。
8)
フローサイトメーターで目的の細胞の蛍光陽性率を測定します。
サンプルはアイスバス中で遮光保存し、24時間以内に測定してください。
測定結果の判定法
【フローサイトメーターによる測定】
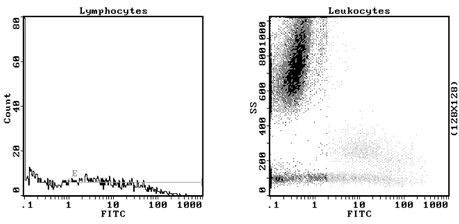
図. ヒストグラム例(健常者末梢血、全血法、EPICS XLで測定)
左:リンパ球領域 右:全白血球(側方散乱 VS. FITC 蛍光)
【測定条件の確認】
使用するフローサイトメーターは、あらかじめ光学系の設定と散乱光及び蛍光の感度調整を行ってください。詳細は機器取扱説明書をご参照ください。
前方散乱光(FS)と側方(90°方向)散乱光(SS)によるスキャッタサイトグラム上で目的とする細胞領域にゲートを設定します。ゲート内解析細胞数を数千個以上とることで、精度の良い分析結果が得られます。
データ解析は、FITC蛍光(Logスケール)ヒストグラムで行います。蛍光陽性分画のカーソルは、コントロール試薬で同様に染色処理したサンプルを対照として設定します。通常は、コントロール試薬の陽性率が2%以下になるようにカーソル位置を設定しますが、腫瘍検体などでは設定が困難なことがあります。コントロール試薬の陽性率が2%を上回る場合、測定結果は誤差を含んでいるおそれがあります。
前方散乱光(FS)と側方(90°方向)散乱光(SS)によるスキャッタサイトグラム上で目的とする細胞領域にゲートを設定します。ゲート内解析細胞数を数千個以上とることで、精度の良い分析結果が得られます。
データ解析は、FITC蛍光(Logスケール)ヒストグラムで行います。蛍光陽性分画のカーソルは、コントロール試薬で同様に染色処理したサンプルを対照として設定します。通常は、コントロール試薬の陽性率が2%以下になるようにカーソル位置を設定しますが、腫瘍検体などでは設定が困難なことがあります。コントロール試薬の陽性率が2%を上回る場合、測定結果は誤差を含んでいるおそれがあります。
図. ヒストグラム例(健常者末梢血、全血法、EPICS XLで測定)
左:リンパ球領域 右:全白血球(側方散乱 VS. FITC 蛍光)

【測定条件の確認】
測定条件が正しいかどうかを確認するには、CYTO-TROL(精度管理用陽性コントロール細胞、製品番号 6604248)または健常者検体を陽性コントロール検体として測定します。
リンパ球サブセット分析の場合、Fcレセプタを介した単球や顆粒球に対する非特異結合は、リンパ球領域を正しくゲーティングすることで除外できます。検体ごとにリンパ球ゲート確認用抗体試薬(IOTest CD45-FITC/CD14-PE、製品番号 A07738)を測定することで、単球を含まない正しいリンパ球領域のゲーティングが可能です。
各検体のリンパ球に対する非特異的な抗体のFc結合を確認するために、陰性対照には適切なコントロール試薬(IOTestアイソタイプコントロール抗体)を使用してください。
リンパ球サブセット分析の場合、Fcレセプタを介した単球や顆粒球に対する非特異結合は、リンパ球領域を正しくゲーティングすることで除外できます。検体ごとにリンパ球ゲート確認用抗体試薬(IOTest CD45-FITC/CD14-PE、製品番号 A07738)を測定することで、単球を含まない正しいリンパ球領域のゲーティングが可能です。
各検体のリンパ球に対する非特異的な抗体のFc結合を確認するために、陰性対照には適切なコントロール試薬(IOTestアイソタイプコントロール抗体)を使用してください。
臨床的意義
白血球には、T細胞、B細胞、単球、顆粒球などがあり、それぞれの細胞群は、機能の異なる亜群(サブセット)に細分され、あるいは異なる分化段階の細胞により構成されています。免疫応答はこれらのサブセットの相互作用及び直接作用により調節されており、それぞれのサブセットは特徴的な細胞表面マーカーを有しています。
細胞融合法の確立により各種モノクローナル抗体が作製されることによって、それを利用して分化や機能の異なるサブセットをその表面マーカーの抗原性の違いにより解析することが可能となりました。白血球サブセットの分析は、白血球の機能的分類及び分化段階の検索はもとより、免疫反応の解析、免疫機能異常の診断や治療においても重要です。さらに、白血病やリンパ腫など造血系の腫瘍においては、腫瘍細胞の系列や分化段階の同定(タイピング)にも有用です。IOテストは、白血球の細胞表面抗原をフローサイトメトリーで分析するためのモノクローナル抗体試薬です。
細胞融合法の確立により各種モノクローナル抗体が作製されることによって、それを利用して分化や機能の異なるサブセットをその表面マーカーの抗原性の違いにより解析することが可能となりました。白血球サブセットの分析は、白血球の機能的分類及び分化段階の検索はもとより、免疫反応の解析、免疫機能異常の診断や治療においても重要です。さらに、白血病やリンパ腫など造血系の腫瘍においては、腫瘍細胞の系列や分化段階の同定(タイピング)にも有用です。IOテストは、白血球の細胞表面抗原をフローサイトメトリーで分析するためのモノクローナル抗体試薬です。
性能
【特異性】
【感度】
【再現性】
本試薬を用いてヒトHLA-DR抗原陽性培養細胞(KM3細胞(1)及びRaji細胞(2))を検体として測定するとき、陽性率は95%以上です。また、ヒトHLA-DR抗原陰性培養細胞(JURKAT細胞(3))を検体として測定したとき、陽性率は0.5%以下です。
(1)
KM3:Non-T、Non-B Leukemia由来培養細胞株
(2)
Raji細胞:Burkitt lymphoma由来培養細胞株
(3)
JURKAT細胞:T-cell Leukemia由来培養細胞株
【感度】
本試薬をPBSにて4倍希釈し、ヒトHLA-DR抗原陽性培養細胞(KM3細胞・Raii細胞)及び健常人検体3例を測定したときの、陽性細胞の割合は本試薬をそのまま用いて測定した場合の±10%範囲内です。
【再現性】
本試薬を用いて健常人検体3例を5回以上同時に測定した場合の、陽性率の変動係数は±5%以内です。
使用上又は取扱い上の注意
取扱上の注意
1.
本製品は、アジ化ナトリウムを0.1%含有しています。アジ化ナトリウムは酸性下で有毒なアジ化水素酸を産生するため、取り扱いに十分注意してください。また、アジ化物の金属性の排水管内への蓄積による爆発の危険性を避けるため、廃棄は多量の流水で希釈して行ってください。
2.
試薬を凍結保存しないでください。
3.
試薬の外観に変化が見られたり、コントロール検体の測定値に大きな変化がある場合は、試薬の劣化が考えられるので使用しないでください。
4.
使用期限を過ぎた試薬を使用しないでください。
5.
検体及び検体に触れた器具類は感染の危険性があるものとして取り扱い、適切な表示及び処理をした後に廃棄してください。
6.
皮膚や粘膜に検体や試薬が触れないように注意してください。ピペットを口で吸引しないでください。
7.
保管やインキュベーション中に試薬を強い光にさらさないでください。
8.
試薬が微生物に汚染されないようご注意ください。
貯蔵方法、有効期間
貯法
2〜8℃
有効期間
12ヶ月 (使用期限は、ボトルに表示があります。)
包装単位
IOテスト FITC標識抗体HLA-DR IOT2a
製品番号 IM0463U 容量 100テスト (2mL)
主要文献
主要文献
1.
Reinherz EL, et al., ed.: 1986. Leukocyte a Typing II. Vol. 1. Springer-Verlag. pp. 303-313.
2.
McMichael AJ, ed: 1987. Leukocyte a Typing III. Oxford University Press. pp. 144-147, 210-214, 234-238, 239-241, 480-484, 579-581, 889-895.
3.
Knapp W. et al., ed: 1989. Leukocyte a Typing IV. Oxford University Press. pp. 36-38, 274-277, 295, 342-343.
4.
Schlossman. SF, et al., ed: 1995. Leukocyte a Typing V. Oxford University Press. pp. 507-509, 515-518, 790-794, 795-798, 1503-1504.
5.
Beverly PCL and Callard RE. : 1981. Eur.J.Immunol 11: 329-334.
6.
Bryan CF, Newman, JT, et al.: 1987. Trans. Proc. 19: 4340-4344.
7.
Clark P, Normansell DE, et al.: 1987. Blood 67: 1600-1606.
8.
Clevers H, Dunlap S and Terhost C: 1988. Eur.J.Immunol. 18: 705-710.
9.
Denning SM, et al.: 1988. J.Immunol. 141: 2980-2985.
10.
Freedman AS and Nadler LM: 1987. Semin. Oncol. 14: 193-212.
11.
Foon KA and Todd RF: 1986. Blood 68: 1-31.
12.
Hannet I, et al.: 1992. Immunology Today 13: 215-218.
13.
Haziot A, et al.: 1993. J.Immunol. 150: 5556-5565.
14.
Keizer G, et al.: 1985. Eur.J.Immunol. 15: 1142.
15.
Kishimoto TK, et al.: 1990. Proc. Natl. Acad. Sci. USA 87: 2244-2248.
16.
Koepke JA and Landay AL: 1989. Clin Immunol Immunopathol 52: 19-27.
17.
Kung P, Goldstein G, et al.: 1979. Science 206: 347-349.
18.
Laffon A, et al.: 1991. J. Clin. Invest. 88: 546-552.
19.
Lanier LL, Le AM, et al.: 1983. J.Immunol. 131: 1789-1796.
20.
Lum LG: 1987. Blood 69: 369-380.
21.
Maissen B, Rebai N, et al.: 1982. Eur.J.Immunol. 12: 739-747.
22.
Nadler LM, Anderson KC, et al.: 1983. J.Immunol. 131: 244-250.
23.
Polk B, Fox R, et al.: 1987. New Engl.J.Med. 316: 61-66.
24.
Rebai N, Maissen B, et al.: 1982. Eur.J.Immunol. 13: 106-111.
25.
Reinherz EL and Schlossman SF : 1980. Cell 19: 821-827.
26.
Reynolds CW and Ortaldo JR: 1987. Immunology Today. 8: 172-174.
27.
Rouas-Freiss N, et al.: 1997. Proc.Natl.Acad.Sci.USA 94: 5249-5254.
28.
Spits, et al.: 1985. Eur.J.Immunol. 15: 88-91.
29.
Tedder TF, et al.: 1985. J.Immunol. 135: 973-979.
30.
Tucker GC, Aoyama H, et al.: 1984. Cell Diff. 14: 223-230.
31.
van Agthoven A, et al.: 1991: Eur.J.Immunol. 1981: 11-18.
32.
van de Velde, et al.: 1991. Nature 351: 662-665.
33.
Warren SM, et al.: 1991: Immunology 72: 150-157.
34.
Wrnke RA, et al.: 1983: New Engl. J. Med. 309: 1275-1281.
35.
Zola H: 1987. Immunology Today 8: 308-315.
製造販売業者の氏名又は名称及び住所
氏名又は名称(製造販売業の種別)
ベックマン・コールター株式会社
第二種医薬品製造販売業
住所等
〒135-0063 東京都江東区有明三丁目5番7号 TOC有明ウエストタワー
電話番号
03-5530-8500
問い合わせ先
氏名又は名称
ベックマン・コールター株式会社
住所等
〒135-0063 東京都江東区有明三丁目5番7号 TOC有明ウエストタワー
電話番号
0120-566-730
その他の安全性情報
備考
一般的名称:B細胞キット