薬効分類名
体外診断用医薬品
一般的注意事項
使用に際してはこの添付文書をよくお読みください。
また、必要な時に読めるように保管しておいてください。
また、必要な時に読めるように保管しておいてください。
承認・届出等
販売名
セロディア−ASK
添付文書管理コード
16000EZZ01148000_A_01
承認番号
16000EZZ01148000
承認年月
昭和60年11月
一般的名称
一般的名称
30493000
抗ストレプトキナーゼ抗体キット
警告記載無し
|
重要な基本的注意記載無し
|
全般的な注意
1.
本試薬は、体外診断用医薬品です。それ以外の目的には使用しないでください。
2.
本試薬は、検体中の溶血性連鎖球菌由来の抗ストレプトキナーゼ抗体を測定する試薬で、溶血性連鎖球菌やストレプトキナーゼを直接測定するものではありません。
3.
本試薬で抗体陽性または保留と判定された場合は、他の検査結果、臨床症状を加味して総合的に判断してください。
4.
A群溶血性連鎖球菌に感染した場合でも抗体が産生されなかったり、産生されていても抗体の量が少ない場合があります。感染が疑われる場合には本試薬の判定結果が陰性であっても、経時的に検査し、また他の検査結果、臨床症状を加味して総合的に判断してください。
5.
*本試薬および検体は、感染の危険性があるものとして十分に注意して取扱ってください。
6.
添付文書以外の使用方法については保証を致しません。
7.
本試薬には、保存剤としてアジ化ナトリウムが含まれています。試薬が誤って目や口に入ったり、皮膚に付着した場合には、水で十分に洗い流すなどの応急処置を行い、必要があれば、医師の手当などを受けてください。
8.
本試薬の使用に際して機器を用いる場合は、本書とあわせ機器の添付文書および取扱説明書を参照してください。
*形状・構造等(キットの構成)
本キットは次の試薬および付属器具から構成されています。
| 包装規格\構成試薬 | A. 溶解用液 (液 状) | B. 血清希釈用液 (液 状) | C. 感作粒子 (凍結乾燥) | D. 未感作粒子 (凍結乾燥) | E. 対照用陽性血清 (凍結乾燥) |
| 10回用×5 | 20mL 1本 | 25mL 1本 | 3.0mL用 5本 | 0.8mL用 3本 | 0.5mL 1本 |
| 50回用×4 | 35mL 2本 | 54mL 2本 | 15.0mL用 4本 | 4.0mL用 2本 | 0.5mL 2本 |
A. 溶解用液(液状)
B. 血清希釈用液(液状)
C. 感作粒子(凍結乾燥)
D. 未感作粒子(凍結乾燥)
E. 対照用陽性血清(凍結乾燥)
感作粒子、未感作粒子および対照用陽性血清の調製に用います。
B. 血清希釈用液(液状)
検体の希釈に用います。
C. 感作粒子(凍結乾燥)
ストレプトキナーゼを感作したゼラチン粒子を凍結乾燥したものです。調製時、ストレプトキナーゼ感作ゼラチン粒子0.9%を含みます。
D. 未感作粒子(凍結乾燥)
タンニン酸処理したゼラチン粒子を凍結乾燥したものです。調製時、未感作ゼラチン粒子0.9%を含みます。
E. 対照用陽性血清(凍結乾燥)
抗ストレプトキナーゼ抗体陽性ヤギ血清を凍結乾燥したものです。調製時、抗体価1:2,560(最終希釈倍数)となるように調製してあります。
*付属器具
| スポイト | 25μL用 | 2本(10回用×5) |
| 25μL用 | 4本(50回用×4) |
感作粒子および未感作粒子の滴下だけに使用します。他の目的には使用しないでください。
使用目的
血清中の抗ストレプトキナーゼ(ASK)抗体価の測定
測定原理
本試薬は、ゼラチンを粒型化した人工担体に、C群溶血性連鎖球菌の菌体外産物であるストレプトキナーゼを吸着させたもので、この感作粒子が検体中の抗ストレプトキナーゼ抗体と反応し、凝集することを応用した粒子凝集反応(Particle Agglutination Test:PA法)試薬です。
そして次のような特徴を持っています。
1.
検査術式が簡単(マイクロタイター法)です。
2.
3時間後に判定できます。
3.
担体に由来する非特異凝集をできる限り除去する目的で、自社開発した人工担体を用いています。
操作上の注意
1.
測定検体の性質、採取法
(1)
可能な限り新鮮な検体を使用してください。検体を保存する場合は−20℃以下で凍結保存してください。
(2)
検体を繰り返し凍結融解することは避けてください。
(3)
検体中に赤血球その他の有形成分が含まれていますと、反応に支障をきたすことがありますので、遠心して除去したのち検査に用いてください。
(4)
検体間の汚染が生じないように検体の取扱いには注意してください。
(5)
血清検体は、56℃で30分間、不活化(非働化)して使用してください。
2.
妨害物質・妨害薬剤
検体に遊離型ビリルビン、抱合型ビリルビン、溶血ヘモグロビンを添加して試験した結果、それぞれ19.1mg/dL、19.6mg/dL、484mg/dLまで測定値に影響は認められませんでした。また、乳びにつきましても2,130ホルマジン濁度まで測定値に影響は認められませんでした。
3.
その他
(1)
感作粒子、未感作粒子および対照用陽性血清は、使用の30分前に所定量の溶解用液にて調製し使用してください。
(2)
感作粒子および未感作粒子は、使用前に均一になるように混和してから使用してください。
(3)
マイクロプレートの内容物は十分に混合してください。
(4)
反応中はマイクロプレートに必ずふたをし、振動を与えないでください。
用法・用量(操作方法)
1.
使用器具
本キットの使用に際しては、次のような器具を用意してください。
| マイクロプレート | U型 |
| ダイリューター | 25μL(0.025mL)用 |
| ドロッパー | 25μL(0.025mL)用 |
| ピペット | マイクロピペットおよびメスピペット |
| プレートミキサー | |
| 判定用ビュアー |
2.
試薬の調製(表1参照)
A. 溶解用液(液状)
B. 血清希釈用液(液状)
C. 感作粒子(凍結乾燥)
D. 未感作粒子(凍結乾燥)
E. 対照用陽性血清(凍結乾燥)
そのまま使用してください。
B. 血清希釈用液(液状)
そのまま使用してください。
C. 感作粒子(凍結乾燥)
溶解用液を所定量加えて調製します。
使用の30分前に室内温度(15〜30℃)にて調製してください。
D. 未感作粒子(凍結乾燥)
溶解用液を所定量加えて調製します。
使用の30分前に室内温度(15〜30℃)にて調製してください。
E. 対照用陽性血清(凍結乾燥)
溶解用液を所定量加えて調製します。
使用の30分前に室内温度(15〜30℃)にて調製してください。
3.
測定操作
(1)
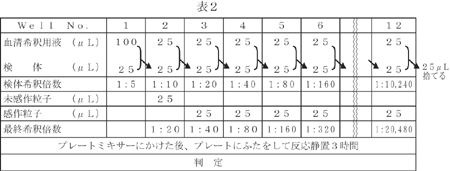
定量法(表2参照)
1)
マイクロプレートU型(8×12穴)を横に使い、1検体に1列(12穴)を用います。
2)
マイクロピペットまたはドロッパーを用いて、血清希釈用液をマイクロプレートの第1穴に100μL(4滴)、また第2穴以降最終穴まで25μL(1滴)ずつ分注します。
3)
マイクロピペットを用いて検体を25μLとり、第1穴に入れます(血清希釈用液100μLが入っている表層に注入します)。
4)
マイクロピペットまたはダイリューターを用い、第1穴から最終穴まで2n希釈を行います。
5)
添付のスポイトを用いて、未感作粒子を第2穴に1滴(25μL)、感作粒子を第3穴以降最終穴まで1滴(25μL)ずつ滴下します。
6)
プレートミキサーなどを用いて、マイクロプレートの内容物が飛び散らない程度の強さで約30秒間混合します。マイクロプレートにふたをして室内温度(15〜30℃)に水平に静置し、3時間後に判定します。なお、翌日まで静置して判定しても差し支えありません。
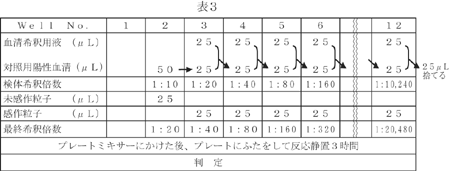
(2)
対照試験(表3参照)キットごとに対照用陽性血清を検体と同様の操作で試験します。すでに10倍に希釈されていますので、まず第3穴以降に血清希釈用液を25μL(1滴)ずつ分注し、次いで第2穴にこの対照用陽性血清を50μLとり、以下は(1)定量法に準じて試験してください。対照用陽性血清は、抗体価1:2,560(最終希釈倍数)となるように調製してあります。
測定結果の判定法
1.
反応像の読み
判定用ビュアーの上にマイクロプレートを静かに置き、粒子の反応像を観察します。反応像はメディウム対照の像と対比して、表4を参照して読んでください。
| 反 応 像 | 読み |
| 粒子がボタン状に集まり、外周縁が均等でなめらかな円形を示すもの。 | (−) |
| 粒子が小さなリングを形成し、外周縁が均等でなめらかなもの。 | (±) |
| 粒子リングが明らかに大きく、その外周縁が不均等で荒く、周辺に凝集の見られるもの。 | (+) |
| 凝集が均一に起こり、凝集粒子が底全体に膜状に広がっているもの。 | (++) |
2.
判定基準
陽 性
陰 性
保 留
未感作粒子(最終希釈倍数1:20)の反応像の読みが(−)で、感作粒子(最終希釈倍数1:40)の反応像の読みが(+)を示すものを陽性とします。反応像の読みが(+)を示した最終希釈倍数をもって抗体価とします。
陰 性
未感作粒子の反応像の読みにかかわらず、感作粒子(最終希釈倍数1:40)の反応像の読みが(−)を示すものを陰性とします。
保 留
未感作粒子(最終希釈倍数1:20)の反応像の読みが(−)で、感作粒子(最終希釈倍数1:40)の反応像の読みが(±)を示すものを判定保留とします。
・判定の際は、以下の点にご注意ください。
(1)
検査ごとに血清希釈用液と感作粒子および未感作粒子の反応像が(−)であることを確かめます(メディウム対照試験)。
(2)
各検体ごとに、未感作粒子の反応(最終希釈倍数1:20)が(−)であることを確かめます。
3.
吸収試験
未感作粒子および感作粒子が共に(±)以上の凝集を示した検体については、次の手順による吸収操作を行った上で再試験をしてください。
(1)
小試験管(スピッツ管など)に所定量の溶解用液で調製した未感作粒子を450μL入れます。
(2)
検体を50μL加えてよく混合し、室内温度(15〜30℃)に少なくとも30分間放置します。(途中1〜2回よく振り混ぜてください)。
(3)
遠心分離(700×g、5分間)し、その上清液〔吸収済み希釈検体(1:10)〕を注意深く分取してマイクロプレートの第2穴に50μLとります。
(4)
第3穴以降はあらかじめ血清希釈用液を25μL(1滴)ずつ分注しておき、第2穴から最終穴までマイクロピペットまたはダイリューターを用いて2n希釈を行います。
(5)
添付のスポイトを用いて、未感作粒子を第2穴に1滴(25μL)、感作粒子を第3穴以降最終穴まで1滴(25μL)ずつ滴下します。
(6)
プレートミキサーなどを用いて、マイクロプレートの内容物が飛び散らない程度の強さで約30秒間混合します。マイクロプレートにふたをして室内温度(15〜30℃)に水平に静置し、3時間後に判定します。なお、翌日まで静置して判定しても差し支えありません。
4.
判定上の注意
免疫血清反応においては、一般的にプロゾーン現象が考えられますので、十分ご留意ください。
臨床的意義
溶血性連鎖球菌の産生する毒素および酵素にはストレプトリジンO、ストレプトキナーゼ、ストレプトドルナーゼ、ヒアルロニダーゼ、ニコチンアミドアデニンジヌクレオチダーゼなどがあり、感染に際しては、これら各々の毒素や酵素に対する抗体の産生が認められ臨床的意義が報告されております。
しかしながら、溶血性連鎖球菌の感染−増殖に伴って産生される代謝産物は菌の病原性、宿主の免疫機構および治療の有無などによって様々な影響を受け、そのため、Stollerman, Wannamaker らは抗体価の測定に際しては特定の抗体に偏ることなく、いくつかの抗体を同時に測定することが、溶血性連鎖球菌感染症の診断をより正確にすると報告しています。
本法は、間接凝集反応を基本原理とした抗ストレプトキナーゼ抗体を検出するための試薬で、溶血性連鎖球菌感染症の血清学的診断と治療に役立てようとするものです。
性能
1.
性能
(1)
正確性試験自家管理検体(陰性4例、陽性6例)を所定の操作法に従って試験するとき、陰性自家管理検体は1:40(最終希釈倍数)未満、陽性自家管理検体は1:40(最終希釈倍数)以上の陽性反応を示します。
(2)
感度試験キットに添付の対照用陽性血清を所定の操作法に従って試験するとき、管理値(最終希釈倍数1:2,560)に対し、±1管以内の陽性反応を示します。
(3)
同時再現性試験同一人が所定の操作法に従って5回繰り返し試験するとき、最頻値に対し±1管以内の陽性反応を示します。
2.
相関性試験成績
陽性検体89例を使用し、対照品との一致率を検討した結果、以下に示す成績が得られました。
検体例数 n=89
±1管以内一致率 94.3%(84/89例)
使用上又は取扱い上の注意
1.
取扱い上(危険防止)の注意
(1)
検体はHIV、HBV、HCVなどの感染の恐れがあるものとして取扱ってください。
(2)
検査にあたっては感染の危険を避けるため使い捨て手袋を着用し、また口によるピペッティングを行わないでください。
(3)
試薬が誤って目や口に入った場合は、水で十分に洗い流すなどの応急処置を行い、必要があれば、医師の手当などを受けてください。
2.
使用上の注意
(1)
本試薬の使用に際して機器を用いる場合は、その添付文書および取扱説明書に従って使用してください。
(2)
外箱および容器の表示をご確認の上、使用期限を過ぎた試薬は使用しないでください。
(3)
試薬は保存条件を守って使用してください。特に凍結しないように注意してください。
(4)
キット内の試薬は正確な反応が得られるように組み合わせてありますので、製造番号の異なる試薬を組み合わせて使用しないでください。
(5)
本試薬は富士レビオ社製FASTECマイクロプレートUを基準に調製してあります。
(6)
キット内の凍結乾燥品は原則として調製当日限りの使用ですが、2〜10℃に保存した場合、7日間安定です。ただし、念のため検査前に対照試験を行ってください。なお、調製後の感作粒子および未感作粒子を保存する場合は、異物が混入しないよう十分注意し、シ−リングフィルムなどで封をしてください。
3.
廃棄上の注意
(1)
本試薬は保存剤として以下のとおりアジ化ナトリウムを含有しています。廃棄する際は爆発性の金属アジドが生成されないように多量の水とともに流してください。
| 溶解用液 | 0.06% |
| 血清希釈用液 | 0.10% |
| 感作粒子 | 0.08%(調製時) |
| 未感作粒子 | 0.16%(調製時) |
| 対照用陽性血清 | 0.16%(調製時) |
(2)
試薬および容器などを廃棄する場合は、各自治体などの廃棄物に関する規定に従って、医療廃棄物または産業廃棄物など区別して処理してください。
(3)
廃液の廃棄にあたっては、水質汚濁防止法などの規制に従って処理してください。
(4)
使用した器具(ピペット、試験管など)、廃液およびサンプリングチップなどは、次亜塩素酸ナトリウム(有効塩素濃度1,000ppm、1時間以上浸漬)、グルタールアルデヒド(2%、1時間以上浸漬)などによる消毒処理あるいは、オートクレーブ(121℃、1時間以上)による滅菌処理を行ってください。
(5)
検体、廃液などが飛散した場合には次亜塩素酸ナトリウム(有効塩素濃度1,000ppm)、グルタールアルデヒド(2%)などによるふき取りを行ってください。
(6)
*消毒処理に使用する次亜塩素酸ナトリウム溶液、グルタールアルデヒド溶液が、皮膚についたり、目に入らないように注意してください。
貯蔵方法・有効期間
1.
貯蔵方法
2〜10℃に保存
2.
有効期間
製造後1年
使用期限については、外箱および容器の表示を参照してください。
*包装単位
1キット 10回用×5
1キット 50回用×4
主要文献
土屋治彦、他:臨床検査機器・試薬、7:417、1984
製造販売業者の氏名又は名称及び住所等
氏名又は名称
富士レビオ株式会社
体外診断用医薬品製造販売業
住所等
*東京都八王子市小宮町51番地
電話番号
0120-292-832
問い合わせ先
氏名又は名称
富士レビオ株式会社 お客様コールセンター
住所等
*東京都港区港南4-1-8 リバージュ品川
電話番号
0120-292-832
その他の安全性情報
企業リンク先
http://www.fujirebio.co.jp/