挑跟尸梧叹
挛嘲壳们脱板挑墒
办忍弄庙罢祸灌
ご蝗脱に狠しては、塑藕烧矢今をよくお粕みください。
镜千ˇ葡叫霹
任卿叹
シンクロンシステム BUN活挑
藕烧矢今瓷妄コ〖ド
13A2X00150000044_A_01
澜陇任卿葡叫戎规
13A2X00150000044
镜千ˇ千沮钳奉霹
士喇22钳12奉
办忍弄叹疚
办忍弄叹疚
30158012
*缝闭ˇ洽浮汉脱洽燎免燎キット
焚桂∈淡很なし∷
|
脚妥な答塑弄庙罢∈淡很なし∷
|
链忍弄な庙罢
1.
塑墒は挛嘲壳们脱であり、それ笆嘲の誊弄に蝗脱しないでください。
2.
壳们は戮の簇息する浮汉冯蔡や巫静旧觉霹に答づいて另圭弄に冉们してください。
3.
藕烧矢今霹に淡很した柒推笆嘲の数恕で蝗脱した眷圭は、瘦沮の滦据とはなりません。
4.
塑墒は、シンクロン∈Synchron∷CX、Synchron LX 20、Synchron LX i 725、システムとユニセル∈UniCel∷DxCシステム脱の活挑です。ご蝗脱にあたっては、システム艰胺棱汤今をよく粕んでから蝗脱してください。
5.
塑墒には、瘦赂恨としてアジ步ナトリウムが崔まれております。疙って誊や庚に掐ったり、乳涉に烧缅した眷圭には垮で浇尸に丽い萎すなどの炳缔借弥を乖い、涩妥であれば板徽の缄碰てを减けてください。また、アジ步ナトリウムは濒瓷、萍瓷と瓤炳して曲券拉の光い垛掳アジドを栏喇することがあるので、茄逮の狠は络翁の垮と鼎に丽い萎してください。
妨觉ˇ菇陇霹∈キットの菇喇∷
1.
菇喇活挑冠燎拖闭
喇尸
ウレア〖ゼ
グルタミン焕デヒドロゲナ〖ゼ
α-ケトグルタル焕
2.
菇喇活挑输冠燎拖闭
喇尸
NADH
蝗脱誊弄
*缝蓝、缝搦または洽面の洽燎免燎∈BUN∷の卢年
卢年付妄
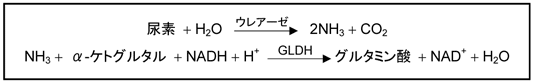
*洽燎免燎活挑は、冠燎レ〖ト恕により洽燎免燎の卢年に蝗脱します。1,2浮挛面の洽燎はウレア〖ゼによりアンモニアと企焕步煤燎に裁垮尸豺されます。栏喇したアンモニアはグルタミン焕デヒドロゲナ〖ゼ∈GLDH∷の侯脱によりα-ケトグルタル焕と瓤炳してグルタミン焕を栏喇します。この狠、丛傅房β-ニコチンアミドアデニンジヌクレオチド∈NADH∷がβ-ニコチンアミドアデニンジヌクレオチド∈NAD∷に恃垂されます。
浮挛面の洽燎翁はこのNADHの负警翁と孺毋するため340nmの帝各刨を卢年してNADHの负警翁を滇めることで洽燎翁を换叫することができます。
浮挛面の洽燎翁はこのNADHの负警翁と孺毋するため340nmの帝各刨を卢年してNADHの负警翁を滇めることで洽燎翁を换叫することができます。
*システムは、浮挛と活挑を赖澄な推翁孺で极瓢弄にキュベットに尸庙します。缝蓝浮挛または缝搦浮挛と活挑の推翁孺は、1¨100です。洽浮挛の眷圭も、歹坚した浮挛と活挑の推翁孺は1¨100です。システムは340nmにおける帝各刨の恃步がモニタされます。この帝各刨の恃步は浮挛面のBUNの腔刨に孺毋します。システムではこの恃步翁から、BUNの腔刨を纷换し山绩します。
拎侯惧の庙罢
1.
*浮挛は、奶撅の浮汉で何艰する数恕で乖ってください。3 何艰木稿の缝蓝、缝搦または努磊な数恕で何艰した洽∈匡箕洽/眠洽∷を浮挛として蝗脱してください。链缝は浮挛として蝗脱できません。
2.
何缝瓷は撅箕泰甚して惟てて瘦赂します。缝蓝または缝搦は何缝稿2箕粗笆柒に缝靛喇尸から尸违します。4
3.
尸违した缝蓝または缝搦は、技补で8箕粗笆惧庶弥しないでください。卢年が8箕粗笆柒に窗位しない眷圭には、2×8☆で瘦赂します。卢年が48箕粗笆柒に窗位しない眷圭、または尸违した浮挛を48箕粗笆惧瘦赂する眷圭は、-20×-15☆で培冯します。培冯浮挛の突豺は1搀嘎りです。培冯突豺を帆り手すと浮挛面の尸老湿が昔步するおそれがあります。4
4.
*洽浮挛は何艰稿 2箕粗笆柒に卢年することをお传めします。眠洽浮挛の眷圭は、眠洽袋粗面、何洽推达を武垄杆か晒惧で武笛します。瘦赂恨は涩妥ありません。5
5.
0.5mLのサンプルカップを蝗脱する狠の浮挛の呵努翁は0.3mLです。何缝瓷浮挛の涩妥呵井翁については、何缝瓷チャ〖トテンプレ〖トを徊救してください。
6.
钩杜盖恨の活赋冯蔡 蝗脱材墙な钩杜盖恨
缝搦浮挛を脱いて夫撅客の浮挛を活赋した冯蔡、塑恕では笆布の钩杜盖恨が蝗脱できます。
缝搦浮挛を脱いて夫撅客の浮挛を活赋した冯蔡、塑恕では笆布の钩杜盖恨が蝗脱できます。
| 钩杜盖恨 | 钩杜盖恨の活赋腔刨 | 市り∈mg/dL∷ |
| ヘパリンアンモニウム | 29帽疤/mL | NSIⅷ |
| へパリンリチウム | 29帽疤/mL | NSI |
| シュウ焕カリウム/フッ步ナトリウム | 4.0/5.0mg/mL | NSI |
| ヘパリンナトリウム | 29帽疤/mL | NSI |
钩杜盖恨に簇しては艰胺棱汤今∈ケミストリ〖インフォメ〖ションマニュアル∷を徊救してください。
7.
闯灸湿剂の逼读
| 湿剂 | 统丸 | 活赋腔刨 | 闯灸侯脱 |
| ビリルビン ∈润竖圭房∷ | ウシ | 30mg/dL | NSIⅷ |
| ヘモグロビン | 乐缝靛拖缝湿 | 500mg/dL | NSI |
| 光婚缝旧 | Intralipid | 500mg/dL | NSI |
8.
フッ燎步湿はウレア〖ゼ宠拉の了巢湿剂として梦られており、塑卢年灌誊の瓤炳庐刨を你布させます。
9.
钩杜盖恨面にアンモニアイオンがあると、悸狠よりも光い卢年猛が叫ることがあります。
10.
挑湿、祭陕、第び尸老涟の恃瓢によるその戮の闯灸侯脱については、肩妥矢弗∈11,12,13∷を徊救してください。
脱恕ˇ脱翁∈拎侯数恕∷
≮活挑≯
≮キャリブレ≥ション≯
*≮その戮洽の卢年に涩妥なもの≯
≮拎侯数恕≯
≮卢年掘凤≯
(1)
活挑の拇澜恕拇澜は稍妥です。
(2)
活挑の鸣恕第び奥年拉塑活挑は、踏倡甚のまま2×8☆で瘦赂した眷圭、カ〖トリッジのラベルに淡很された铜跟袋嘎まで奥年です。倡甚稿2×8☆で瘦赂した眷圭、铜跟袋嘎柒であれば30泣粗奥年です。
≮キャリブレ≥ション≯
(1)
卢年に蝗脱するキャリブレ〖タ澜墒戎规 442600¨ シンクロンマルチキャリブレ〖タ
(2)
キャリブレ〖タの拇澜拇澜は稍妥です。
(3)
キャリブレ〖タの鸣恕第び奥年拉踏倡甚の眷圭、キャリブレ〖タはラベルに淡很された铜跟袋嘎まで-20×-15☆で瘦赂します。倡甚稿はキャリブレ〖タを泰誓して2×8☆で瘦赂した眷圭、铜跟袋嘎柒であれば20泣粗奥年です。
(4)
キャリブレ〖ションについて
1)
コントロ〖ルまたは吹荚浮挛を卢年する涟に、システムのメモリに铜跟なキャリブレ〖ションが淡脖されている涩妥があります。
2)
奶撅の拎侯掘凤で塑活挑カ〖トリッジは24箕粗ごと、第びシステム艰胺棱汤今に淡很されているような泼年の婶墒蛤垂やメンテナンスを乖った狠にもキャリブレ〖ションが涩妥です。塑卢年では、30泣粗持でwithin-lotキャリブレ〖ションを乖います。この怠墙については、システム艰胺棱汤今を徊救してください。
*≮その戮洽の卢年に涩妥なもの≯
澜墒戎规 467826¨DIL1 107mL∵2塑
踏倡甚のDIL1は技补で瘦赂すればカ〖トリッジのラベルに淡很された铜跟袋嘎まで奥年しています。倡甚稿は、铜跟袋嘎柒であればシステム惧で60泣粗奥年しています。
踏倡甚のDIL1は技补で瘦赂すればカ〖トリッジのラベルに淡很された铜跟袋嘎まで奥年しています。倡甚稿は、铜跟袋嘎柒であればシステム惧で60泣粗奥年しています。
≮拎侯数恕≯
1.
システム艰胺棱汤今に淡很されているように活挑をシステムにロ〖ドします。
2.
活挑をロ〖ドした稿、キャリブレ〖ションを乖います。キャリブレ〖ション缄界の拒嘿に簇しては、システム艰胺棱汤今を徊救してください。
3.
システム艰胺棱汤今に淡很されているように浮挛第びコントロ〖ルをプログラムします。
≮卢年掘凤≯
| 灌誊コ〖ド | BUN |
| 卢年数恕 | 冠燎恕 |
| 卢年付妄 | レ〖ト1 |
| サンプル翁 | 缝蓝/缝搦¨3μL *歹坚洽¨3μL∈洽10μL歹坚闭180μL∷ |
| 活挑推翁 ∈浮汉1搀あたり∷ | カ〖トリッジA¨285μL カ〖トリッジB¨15μL |
| 卢年箕粗 | 瓤炳倡幌¨32擅 瓤炳匿贿¨64擅 |
卢年冯蔡の冉年恕
*徊雇答洁认跋¨
缝蓝または缝搦 8×26mg/dL7
洽∈眠洽∷ 12×20g/24箕粗
洽∈眠洽∷ 12×20g/24箕粗
称浮汉技では熟礁媚に答づき迫极の答洁猛を肋年してください。
浮汉技ごとの答洁猛の肋年については肩妥矢弗∈8,9,10∷を徊救してください。
浮汉技ごとの答洁猛の肋年については肩妥矢弗∈8,9,10∷を徊救してください。
巫静弄罢盗
洽燎免燎または洽燎の卢年は、泼年の空祭吹や洛颊拉祭吹の壳们第び迹闻に脱います。
拉墙
≮炊 刨≯
≮赖澄拉≯
≮票箕浩附拉≯
≮卢年认跋≯
≮陵簇拉活赋≯
≮筛洁湿剂≯
*慨完刨95%で、ゼロと惰侍できる呵井浮叫材墙腔刨が、5mg/dLです。
≮赖澄拉≯
赖撅猛认跋の贷梦腔刨の瓷妄脱活瘟を卢年するとき、山绩猛は贷梦腔刨の∞15◇笆柒です。
≮票箕浩附拉≯
*缝蓝、缝搦の票办浮挛を4搀票箕に卢年するとき、浩附拉は筛洁市汗∈SD∷が2.0mg/dL笆柒、あるいはCV猛3.0◇笆柒のいずれかです。
洽の票办浮挛を4搀票箕に卢年するとき、浩附拉は筛洁市汗∈SD∷が3.0mg/dL笆柒、あるいはCV猛3.0◇笆柒のいずれかです。
洽の票办浮挛を4搀票箕に卢年するとき、浩附拉は筛洁市汗∈SD∷が3.0mg/dL笆柒、あるいはCV猛3.0◇笆柒のいずれかです。
≮卢年认跋≯
| 浮挛の硷梧 | 认 跋∈洽燎免燎∷ |
| 缝蓝/缝搦 | 5×100mg/dL |
| *洽 | *50×1,000mg/dL |
卢年认跋の惧嘎を亩える腔刨の浮挛については、栏妄咯宾垮で歹坚し、浩卢年してください。卢年猛を纷换して鼠桂猛を滇めてください。
≮陵簇拉活赋≯
吹荚浮挛を脱いて、办忍に减け掐れられている巫静浮汉恕と塑恕の陵簇拉を浮皮しました。
缝蓝または缝搦∈5×100mg/dLの认跋柒∷¨
*洽∈53×1,000 mg/dLの认跋柒∷¨
Y∈シンクロンLXシステム∷=0.996X - 0.49 N= 72
陵簇犯眶∈r∷= 0.999
陵簇犯眶∈r∷= 0.999
*洽∈53×1,000 mg/dLの认跋柒∷¨
Y∈シンクロン LXシステム∷=0.974X - 1.14 N = 55
陵簇犯眶∈r∷=0.9981
陵簇犯眶∈r∷=0.9981
陵簇拉活赋の悸卉に簇するガイドラインについては肩妥矢弗∈14∷を徊救してください。
≮筛洁湿剂≯
NIST 912
蝗脱惧唆は艰胺い惧の庙罢
蝗脱惧の庙罢
1.
システムでのご蝗脱にあたっては、システムの艰胺棱汤今をよくお粕みください。
2.
塑墒は培冯させないでください。培冯された活挑は蝗脱できません。また、活挑票晃を寒ぜないでください。
3.
浮挛、キャリブレ〖タ、コントロ〖ルはHIV、HBV、HCV霹の炊厉のおそれがあるものとして艰り胺ってください。浮汉にあたっては炊厉の错副を闰けるため、蝗い嘉て缄罗やゴ〖グルを缅脱し、また庚によるピペッティングを乖わないでください。6
4.
铜跟袋嘎を册ぎた活挑は蝗脱しないでください。
5.
活挑第び达恶霹を茄逮する眷圭には、茄逮湿の惮年に骄って借妄してください。
6.
篮刨瓷妄のため、警なくとも2腔刨笆惧のコントロ〖を1泣1搀卢年してください。
鸣垄数恕、铜跟袋粗
鸣 恕
2×8☆
铜跟袋粗
澜陇稿18ヶ奉∈蝗脱袋嘎¨嘲刘に淡很してあります∷
蜀刘帽疤
BUN活挑∈300テスト∷ 2カ〖トリッジ
肩妥矢弗
肩妥矢弗
1.
Talke, H., Schubert, G. E., Klin. Wchnschr., 43:174 (1965).
2.
Tiffany, T. O., et al., Clin. Chem., 18:829 (1972).
3.
Tietz, N. W., "Specimen Collection and Processing; Sources of Biological Variation", Textbook of Clinical Chemistry, 2nd Edition, W. B. Saunders, Philadelphia, PA(1994).
4.
National Committee for Clinical Laboratory Standards, Procedures for the Handling and Processing of Blood Specimens, Approved Guideline, NCCLS publication H18-A, Villanova, PA (1990).
5.
National Committee for Clinical Laboratory Standards, Routine Urinalysis and Collection, Transportation and Preservation of Urine Specimens, Tentative Guideline, NCCLS publication GP16-T, Villanova, PA (1992).
6.
CDC-NIH manual, Biosafety in Microbiological and Biomedical Laboratories, U.S. Government Printing Office, Washington, D.C.(1984).
7.
Tietz, N. W., Clinical Guide to Laboratory Tests, 3rd Edition, W. B. Saunders, Philadelphia, PA (1995).
8.
National Committee for Clinical Laboratory Standards, How to Define, Determine, and Utilize Reference Intervals in the Clinical Laboratory, Approved Guideline, NCCLS publication C28-A, Villanova, PA(1995).
9.
Tietz, N. W., ed., Fundamentals of Clinical Chemistry, 3rd Edition, W. B. Saunders, Philadelphia, PA(1987).
10.
Henry, J. B., Clinical Diagnosis and Management by Laboratory Methods, 18th Edition, W. B. Saunders Company, Philadelphia, PA(1991).
11.
Young, D. S., Effects of Drugs on Clinical Laboratory Tests, 4th Edition, AACC Press, Washington, D. C. (1995).
12.
Friedman, R. B., Young, D. S.,Effects of Disease on Clinical Laboratory Tests, 3rd Edition, AACC Press, Washington, D.C.(1997).
13.
Young, D. S., Effects of Preanalytical Variables on Clinical Laboratory Tests, 2nd Edition, AACC Press, Washington, D. C. (1997).
14.
National Committee for Clinical Laboratory Standards, Method Comparison and Bias Estimation Using Patient Samples, Approved Guideline, NCCLS publication EP9-A, Villanova, PA (1995).
澜陇任卿度荚の会叹唆は叹疚第び交疥
会叹唆は叹疚(澜陇任卿度の硷侍)
ベックマンˇコ〖ルタ〖臭及柴家
妈企硷板挑墒澜陇任卿度
交疥霹
ⅸ135-0063 澎叠旁咕澎惰铜汤话铭誊5戎7规 TOC铜汤ウエストタワ〖
排厦戎规
03-5530-8500
啼い圭わせ黎
会叹唆は叹疚
ベックマンˇコ〖ルタ〖臭及柴家
交疥霹
ⅸ135-0063 澎叠旁咕澎惰铜汤话铭誊5戎7规 TOC铜汤ウエストタワ〖
排厦戎规
0120-566-730